西安交大科研人员提出 基于硅基弹性-基因激活生物活性材料的骨组织再生新策略
硅基生物活性医用材料如生物活性玻璃、硅酸盐陶瓷等是一类重要的生物医用材料,具有优越的骨整合能力、成骨诱导活性、创面修复活性和生物安全性,在骨组织再生与替代、软组织创面修复、药物基因递送等方面具有重要的应用潜力和价值。然而传统硅基生物活性材料力学脆性大、弹性差、降解慢,大大限制了该类生物医用材料的再生医学应用范围。开发具有仿生弹性、可控生物降解、组织诱导活性的新型硅基生物活性材料对促进组织修复与再生的效率具有重要的意义。
西安交通大学材料学科-生物医学工程学科/生物诊断治疗国家地方联合工程研究中心雷波教授团队一直致力于具有疾病治疗和组织再生作用高性能硅基生物活性杂化材料的设计与应用研究。2015年在国际上合成出了基于柠檬酸的生物活性聚硅柠檬酸酯分子杂化弹性材料(Adv.Funct.Mater.2015,25,5016),发现了该材料内在的多功能特性(高弹性,光致发光,抗菌,成骨分化),实现其中生物成像(Adv. Healthcare Mater, 2016, 5, 382; Appl. Mater. Today, 2018, 10, 153),材料体内示踪(ACS Appl. Mater. Interfaces, 2018, 10, 17722), 肿瘤诊疗(Biomaterials, 2019,201,68), 组织快速修复再生(Adv. Funct. Mater, 2020, 30, 1906013), 示踪-肿瘤治疗-组织修复一体化(ACS Nano, 2020, 14, 2904)等方面的潜在应用。
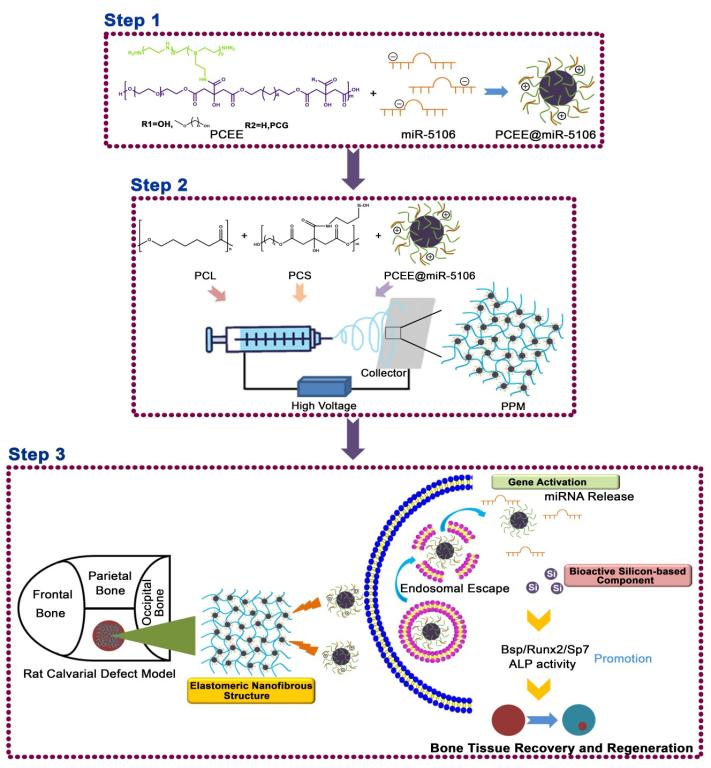
近期,该研究团队针对目前临床骨科对高性能骨修复与再生材料的重大需求,基于弹性聚硅柠檬酸酯材料,设计了一种具有仿生弹性和控释成骨活性miRNA的纳米纤维支架骨修复材料,提出利用弹性(物理)/硅释放(化学)/miRNA控释(生物)协同促进骨组织再生的新策略(图1)。该生物活性材料采用弹性硅基柠檬酸分子杂化纳米纤维增强的聚己内酯为仿生弹性骨架,内置聚柠檬酸酯-miRNA的纳米复合物,实现了光致发光、纳米结构、弹性、硅基活性组分、长期miRNA释放的多重功能效应,体外实验发现该材料可以高效促进干细胞成骨分化,体内骨缺损模型进一步验证了该弹性硅材料体系促进骨组织快速修复和重建的能力。该研究可能为骨缺损的治疗提供了一种简单有效的生物活性材料的多因素协同思路。
以上研究成果以“Biomimetic Elastomeric Bioactive Siloxane-Based Hybrid Nanofibrous Scaffolds with miRNA Activation: A Joint Physico-Chemical-Biological Strategy for Promoting Bone Regeneration”为题发表在材料领域著名期刊 Advanced Functional Materials上(Adv.Funct.Mater., 2020, 30, 1906013,影响因子16.8)。雷波教授为该论文的唯一通讯作者,西安交通大学为该论文的唯一通讯单位。该研究工作得到了西安交通大学“青年拔尖人才支持计划”、“双一流”大学建设先导项目、国家自然科学基金重点项目、国家自然科学基金面上项目、陕西省颅颌面精准医学研究重点实验室等项目的支持。